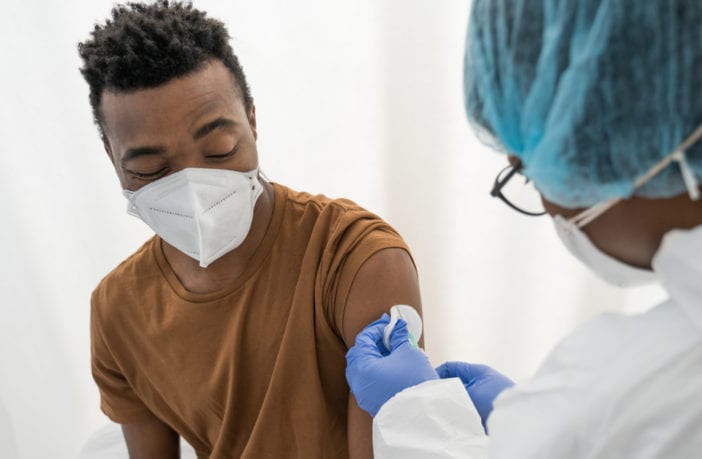
Agência afirma que 'todas as vacinas autorizadas no Brasil garantem proteção contra doença grave e morte'
Após autorizar uma nova pesquisa sobre a aplicação de uma 3ª dose contra a Covid-19, desta vez com pedido feito pela AstraZeneca, a Agência Nacional de Vigilância Sanitária (Anvisa) esclareceu, na última quarta-feira (14), que “ainda não há estudos conclusivos sobre a necessidade” de mais uma aplicação dos imunizantes disponíveis no Brasil.
De acordo com a agência, dois pedidos foram feitos até o momento para estudos sobre a dose adicional.
Além, então, das duas aplicações já previstas em bula.
A Pfizer foi a primeira farmacêutica a conseguir a autorização, ainda em 18 de junho.
Já a AstraZeneca conseguiu a liberação nesta quarta-feira.
Sobre os estudos de 3ª dose liberados pela Anvisa:
- Pfizer: investiga os efeitos, a segurança e o benefício de uma dose de reforço da sua vacina, a Comirnaty. O imunizante extra será aplicado em pessoas que tomaram as duas doses completas há pelo menos seis meses.
- AstraZeneca: a farmacêutica desenvolveu uma segunda versão da vacina que está em uso no país, buscando proteção contra a variante beta. Parte do ensaio clínico prevê que uma dose da nova versão da vacina (AZD2816) seja aplicada em pessoas que receberam as duas doses da versão atual da AstraZeneca (AZD1222).
” Até agora, todas as vacinas autorizadas no Brasil garantem proteção contra doença grave e morte, conforme os dados publicados”, disse a nota da reguladora.
Dose extra em SP
Na última sexta-feira (9), o governador de São Paulo, João Doria, e o diretor do Instituto Butantan, Dimas Covas, participaram do início dos testes clínicos da ButanVac.
De acordo com Doria, a expectativa é que ela possa ser aplicada a partir de 2022, quando, então, a população deverá ser vacinada novamente contra o vírus, em uma terceira dose.
O diretor do Butantan afirmou que 10 milhões de doses já foram, portanto, produzidas para distribuição.
E que isso acontecerá, então, após a conclusão dos testes e autorização da Anvisa para aplicação.
“Já temos o equivalente a mais de dez milhões de doses prontas, aguardando, então, os resultados iniciais desse estudo clínico para definir como serão as próximas fases e qual será a confirmação final da vacina”.
Queiroga diz que País já tem oferta suficiente de vacina e descarta Covaxin e Sputnik V
Fonte: G1
Foto: Shutterstock