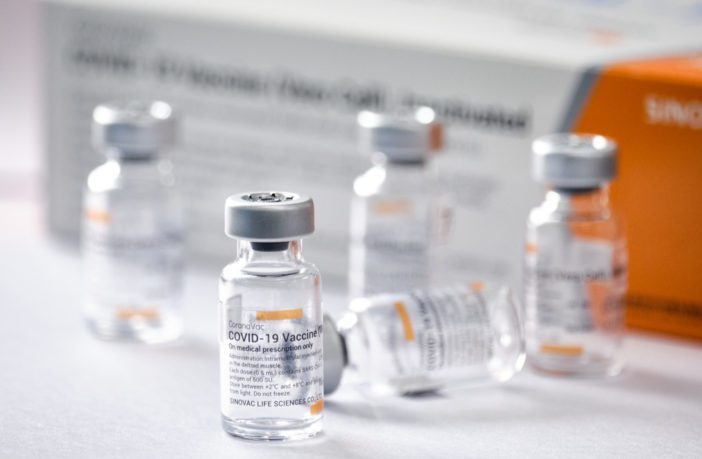
O Instituto Butantan já tem armazenado 10 milhões de doses prontas
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou hoje a liberação do uso da vacina contra a covid-19 CoronaVac em crianças e jovens de 6 a 17 anos. Por unanimidade, os cinco diretores do órgão votaram favoravelmente à aprovação durante videoconferência para avaliar um pedido para uso emergencial do imunizante feito pelo Instituto Butantan.
Inicialmente, o Butantan pediu autorização para vacinar crianças a partir de 3 anos.
No entanto, a Anvisa alegou falta de estudos suficientes que comprovem a eficácia para essa faixa de idade, e decidiu validar a aplicação da vacina da CoronaVac apenas em crianças com idade a partir de 6 anos.
Na prática, a faixa etária que pode ser vacinada no Brasil não muda, mas, com a aprovação da CoronaVac para crianças, haverá oferta maior de vacinas.
A saber, o Instituto Butantan já tem armazenado 10 milhões de doses prontas.
Até hoje, apenas a vacina da Pfizer estava liberada para crianças a partir de 5 anos.
Todavia, as doses vêm desembarcando no Brasil em remessas vindas do exterior em quantidade ainda insuficiente para imunizar todas as faixas de idade infantil.
Como será a vacina da CoronaVac para crianças e jovens?
- Mesma formulação aplicada em adultos.
- Mesma dose adulta: 600 SU em 0,5 mL.
- Duas doses no intervalo entre 2 e 4 semanas.
- Faixa etária: 6 a 17 anos.
- Não aplicar em crianças imunocomprometidas, ou seja, com baixa imunidade.
O ministro da Saúde, Marcelo Queiroga, afirmou na última terça-feira que a CoronaVac para crianças seria incluída no plano nacional de imunização se fosse aprovada, mas a questão ainda será analisada pela pasta.
Logo após a aprovação, o governador de São Paulo, João Doria (PSDB), disse que iniciaria “imediatamente a vacinação” no estado. “Esperamos imunizar toda garotada em, no máximo, 3 semanas”, escreveu em suas rede sociais.
Como foram os votos que aprovaram a CoronaVac para crianças
Responsável por estudar os documentos enviados pelo Instituto Butantan, a Gerencia-Geral de Medicamentos recomendou aos diretores da Anvisa a aprovação do uso da CoronaVac em crianças.
“A totalidade das evidências cientificas sugerem que há beneficio e segurança para uso na população pediátrica”, afirmou o gerente-geral de Medicamentos, Gustavo Mendes, que lembrou não haver “tratamentos medicamentosos aprovados para população abaixo de 12 anos”.
Antes de seu voto, a diretora e relatora do tema, Meiruze Sousa Freitas, lembrou, também, que a vacina aprovada da Pfizer “não está em quantidade suficiente para atender a demanda no primeiro trimestre: 20 milhões de crianças com duas doses”.
Sobre o voto, a relatora afirmou ter levado em consideração a avaliação dos setores técnicos da Anvisa e a opinião das sociedades médicas consultadas, que “permitiu a essa relatoria que, ressalvadas incertezas ainda existentes, os benefícios potenciais da CoronaVac superam os riscos potencias inerentes a essa vacina. Dessa forma, estou convicta de que ela atende aos critérios necessários para o uso emergencial pediátrico de 6 a 17 anos em crianças não imunocomprometidas.”
Histórico
O Butantan já havia tentado a liberação do imunizante para crianças em julho do ano passado.
Na ocasião, contudo, a Anvisa rejeitou o pedido, argumentando que ainda faltavam dados sobre a eficácia e a segurança da vacina para o público-alvo.
Em janeiro deste ano, a Anvisa passou a apreciar um segundo pedido do Butantan, a partir, então, de novas informações enviadas pelo instituto.
Na semana passada, então, técnicos da agência se reuniram com infectologistas e pesquisadores do Chile, país onde o imunizante já vem sendo aplicado em crianças.
Covid-19: pandemia não está nem perto do fim, adverte OMS
Fonte: Uol
Foto: Shutterstock
.. –