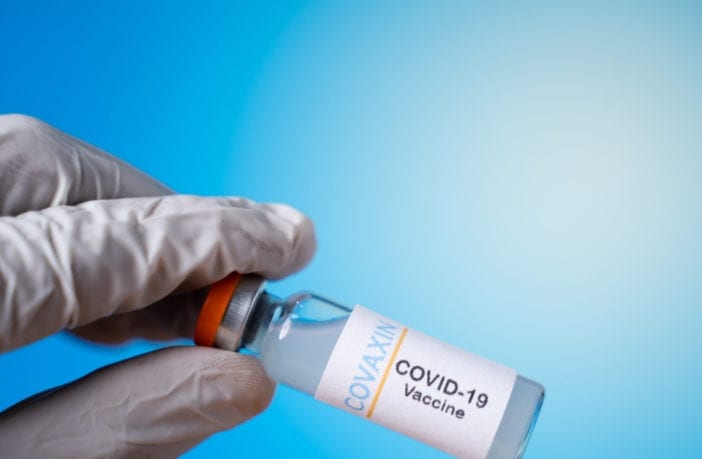
Sua aprovação gerou críticas sobre falta de transparência dos dados de estudos clínico
A Associação Brasileira das Clínicas de Vacinas (ABCVAC) anunciou no último domingo (3) que negocia a compra de cinco milhões de doses da vacina indiana Covaxin contra a Covid-19.
O imunizante é fabricado na Índia pela farmacêutica Bharat Biotech em parceria com o Instituto Nacional de Virologia do país.
No sábado, 2, a vacina recebeu autorização de uso emergencial na Índia e gerou, contudo, críticas de especialistas pela falta de transparência na divulgação dos dados dos ensaios clínicos.
Interesse brasileiro na vacina indiana
A Covaxin faz parte do plano nacional de vacinação do Brasil.
No documento, o governo federal diz ter firmado um memorando de entendimento, não vinculante, para demonstrar a intenção de compra da vacina.
De acordo com o plano, o Ministério da Saúde (MS) aguarda retorno da empresa sobre quantitativo de doses disponíveis e cronograma de entrega.
Todavia, em novembro, a Bharat Biotech apresentou uma proposta de transferência de tecnologia para a produção da vacina indiana no País.
Na última segunda-feira (4), o Ministério da Saúde informou que a rede privada também deve seguir a ordem de vacinação de grupos prioritários prevista no plano nacional de imunização.
Por isso, mesmo que possa vender o produto, as clínicas deverão oferecer primeiro a idosos e profissionais específicos.
Além disso, em nota, a Bharat Biotech disse que iniciou procedimentos junto à Anvisa para “submissão contínua” dos resultados.
No entanto, não há nada acertado ainda com a agência.
A empresa deve apresentar os dados das pesquisas em etapas, mesmo antes de finalizar todos os estudos.
Ela também precisará trazer estudos clínicos ao Brasil para usar a submissão contínua, o que não foi ainda sinalizado para a Anvisa.
Como a Covaxin é produzida?
A tecnologia por trás da vacina tem como base o coronavírus inativado, incapaz de se reproduzir e, portanto, não causa a doença.
O sistema imunológico, ao detectar a presença do vírus, desencadeia a produção de anticorpos e protege o indivíduo contra a doença.
O imunizante pode ser armazenado em temperaturas comuns, de 2ºC a 8ºC, assim, facilitando a logística de distribuição em países como o Brasil.
A vacina é segura?
Em artigo publicado na plataforma medRxiv, ainda em versão pré-print , com dados preliminares das fases 1 e 2 de estudos clínicos da Covaxin, os pesquisadores concluem que o perfil de segurança da vacina é “tolerável” e notavelmente menor que os índices de outros imunizantes contra a Covid-19.
Então, nenhum evento adverso grave relacionado à vacina foi registrado entre os participantes.
O resultado dos estudos ainda não foi publicado em revistas científicas.
Contudo, o órgão regulador de medicamentos da Índia disse que a vacina foi administrada – até o momento – em 22,5 mil voluntários e é segura.
A Covaxin é capaz de gerar resposta imune?
No mesmo artigo, os pesquisadores dizem que na fase 1 de testes, que envolveu 375 voluntários, a BBV152 (nome técnico da vacina) produziu altos níveis de anticorpos neutralizantes que continuaram elevados nos três meses após a aplicação da segunda dose.
Já na fase 2, a vacina aumentou as respostas imunes geradas por anticorpos.
Em comunicado, a Bharat Biotech diz que a Covaxin produz respostas imunológicas de longo prazo contra “múltiplas proteínas virais, não apenas à proteína spike” e capacidade neutralizante que pode reduzir ou eliminar mutações.
Qual é a eficácia da Covaxin?
A farmacêutica ainda não divulgou os dados de eficácia da vacina. Apesar de ter aprovado o uso emergencial do imunizante, a Organização Central de Controle de Medicamentos da Índia não se pronunciou sobre a eficácia da Covaxin. De acordo com uma fonte da agência Reuters, o imunizante pode ser mais de 60% eficaz com um regime de aplicação de duas doses.
Por que a aprovação de uso emergencial na Índia tem sido criticada?
Durante o anúncio da aprovação da Covaxin – divulgada junto de outro aval, o da vacina de Oxford – V.G. Somani, general de controle de medicamentos da Índia, disse que a decisão de liberar as vacinas foi feita após “análises cuidadosas”.
No entanto, de acordo com o órgão regulador de medicamentos da Índia, a Covaxin foi aprovada “para uso restrito em situação de emergência, por interesse público e como precaução, ainda em testes clínicos, especialmente no contexto de infecções por mutações da cepa (do vírus)”.
A All India Drug Action Network (AIDAN), rede independente de fiscalização da saúde pública, divulgou um comunicado solicitando mais informações sobre o escopo dos testes clínicos e regimes de dosagem para as duas vacinas.
Sobre o aval para a Covaxin, a AIDAN disse estar “perplexa” e busca entender “qual lógica científica” motivou os especialistas a autorizar o imunizante ainda em testes clínicos.
Em que fase estão os estudos clínicos?
Cerca de 23 mil voluntários acima de 18 anos fazem parte da última fase de testes clínicos, que determina a eficácia da vacina.
Ainda em andamento, a fase 3 teve início recentemente, no dia 16 de novembro, e é o maior teste conduzido para qualquer vacina na Índia.
A Bharat Biotech tem como meta recrutar mais 3 mil voluntários.
Desde quando a vacina está sendo desenvolvida?
Em julho, foi vazada uma carta escrita por uma autoridade do Instituto Nacional de Virologia indiano (que produz a vacina em parceria com a Bharat Biotech) que mencionava a intenção de lançar uma vacina contra o coronavírus em 15 de agosto, dia da independência da Índia.
A proximidade da data gerou, assim, questionamentos de especialistas em saúde.
No mesmo dia, a Bharat Biotech anunciou a meta de produzir 300 milhões de doses da Covaxin caso os testes clínicos tivessem sucesso.
Quais outros países demonstraram interesse na vacina?
De acordo com a Bharat Biotech, a empresa conversa com representantes de mais de 10 países sobre a possibilidade de compra da vacina.
Nos Estados Unidos, por exemplo, farmacêutica fechou parceria com a biofarmacêutica Ocugen, que vai co-desenvolver a vacina para o mercado americano.
O que é necessário para o uso ser aprovado no Brasil?
Para ser aplicada, a Covaxin deve, então, ser registrada ou receber aval para uso emergencial no Brasil.
A fabricante da vacina precisa pedir essas permissões à Anvisa.
Em nota enviada à reportagem do Estadão, a Bharat Biotech disse que iniciou procedimentos junto à Anvisa para “submissão contínua” dos resultados.
A saber, não há nada acertado ainda com a agência.
Por este caminho, a empresa deve, então, apresentar os dados das pesquisas em etapas, mesmo antes de finalizar todos os estudos.
Além disso, a farmacêutica precisa também trazer estudos clínicos ao Brasil para usar a submissão contínua, o que não foi ainda sinalizado para a Anvisa.
Clínicas privadas brasileiras negociam compra da vacina Covaxin da Índia
Fonte: Estadão
Foto: Shutterstock