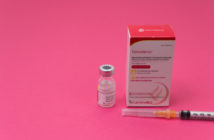
Com armazenamento em refrigerador comum e aplicação de dose única, a vacina também pode ser usada como dose de reforço ou na intercambialidade para elevar a imunidade contra o novo coronavírus
A biofarmacêutica brasileira Biomm, pioneira em medicamentos biotecnológicos no país, solicitou à Agência Nacional de Vigilância Sanitária (Anvisa) autorização para uso emergencial do imunizante Convidecia, da CanSino Biologics INC.
Dessa maneira, a iniciativa visa ampliar a disponibilidade de imunizantes contra a Covid-19 no Brasil.
Com aplicação em dose única e armazenamento em geladeira comum (entre 2 e 8 graus Celsius), o imunizante desenvolvido pela CanSino Biologics INC vem sendo adotado por diversos mercados.
Com aprovações em países como México, Paquistão, Hungria, Chile, Equador, Argentina, Malásia, Indonésia e Quirguistão.
A Convidecia também tem potencial para ser usada como dose de reforço ou na intercambialidade (mix) de vacinas para elevar a imunidade contra o novo coronavírus.
O imunizante é recomendado para ser administrado em pessoas a partir dos 18 anos de idade.
De acordo com a CanSino Biologics INC, a Convidecia tem eficácia geral de 68,83% na prevenção de todos os casos após 14 dias da aplicação.
Portanto, para casos graves de Covid-19, a eficácia da vacina é de 95,47% no mesmo período.
Já os estudos clínicos foram conduzidos no Paquistão, Rússia, Chile, Argentina e México.
“A Biomm começará o processo de importação do imunizante tão logo todas as exigências regulatórias sejam atendidas. Futuramente, também temos a possibilidade produzir a Convidecia na nossa fábrica em Nova Lima (MG), que recebeu investimentos de US﹩ 90 milhões e está em processo de validação”, destaca o CEO da Biomm, Heraldo Marchezini.
O acordo prevê, também, o propósito de comercialização e produção de outras vacinas do portfólio da CanSino Biologics INC.