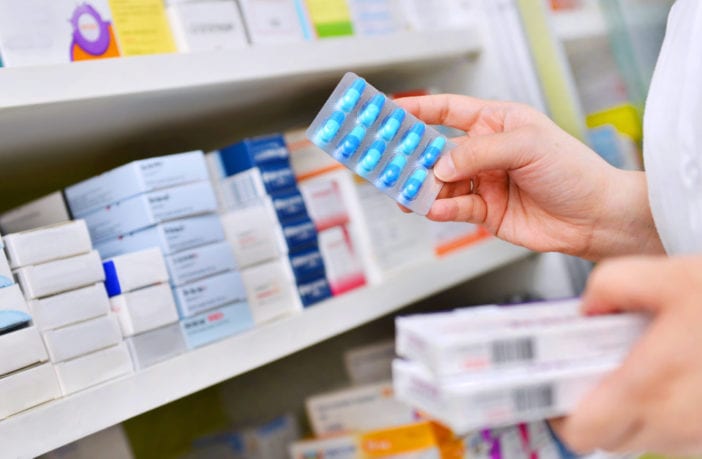
Para perder a obrigatoriedade da prescrição médica, um medicamento precisa de longos anos de mercado; esta exigência faz com que seja difícil inovar no segmento de MIPs e isto aumenta a disputa entre produtos com o mesmo princípio ativo
Disputa mercadológica é o que define a categoria de Medicamentos Isentos de Prescrição (MIPs). A maioria dos produtos não tem patente, logo, enfrenta forte competição de preço. Para confirmar esse cenário, basta observar as gôndolas de uma farmácia. Para os males mais comuns, como gripes e resfriados, é possível encontrar facilmente mais de dez marcas com o mesmo princípio ativo, mas com apresentações, formatos e fórmulas diferenciadas.
Em meio a tantas opções disponíveis, o consumidor tem a liberdade de escolha. Não precisar levar a marca que obrigatoriamente o médico indicou, como ocorre com os controlados.
Todos os MIPs colocados à venda têm segurança e qualidades atestadas pela Agência Nacional de Vigilância Sanitária (Anvisa), então o paciente opta por aquela marca em que mais confia ou que tem o preço que cabe no seu bolso. Esse dinamismo só faz acirrar a disputa entre os laboratórios.
O reflexo disso pode ser observado pelo crescimento constante nos investimentos em comunicação e no varejo que o mercado de MIPs tem apresentado.
Nos últimos anos, os fabricantes aumentaram os aportes em mídia em 41%, segundo dados do Instituto Brasileiro de Opinião Pública e Estatística (Ibope) Monitor. Mas afinal, se a concorrência é feroz, por que as indústrias insistem em lançar MIPs com mesmo princípio ativo e, muitas vezes, versões dos já consagrados entre a população?
De acordo com o presidente executivo do Sindicato da Indústria de Produtos Farmacêuticos no Estado de São Paulo (Sindusfarma), Nelson Mussolini, as exigências necessárias para que um medicamento torne-se livre de prescrição médica explicam parte dessa dinâmica concorrencial peculiar.
“Em tese, você não vai encontrar em um MIP inovador – talvez só alguma forma de apresentação diferenciada –, porque um medicamento só vira isento de prescrição depois de um longo período de mercado, em que demonstra que os efeitos colaterais são pequenos e facilmente detectáveis. Só depois disso, o fabricante pede o switch, ou a mudança de medicamento de prescrição para isento”, conta.
Pela falta de flexibilidade de ser inovador quando se trata de MIPs é que existem tantos produtos para o mesmo fim e o investimento em propaganda precisa ser massivo.
“Em termos de disputa comercial, o MIP é um bem de consumo normal. Óbvio que tomando todos os cuidados com a saúde. Não é um produto de uso indiscriminado. É preciso cuidado, como com todo produto que você estiver ingerindo. E essa consciência se obtém por meio da informação, por isso a publicidade é importante. Sem ela, o risco de haver algum dano é muito maior”, complementa Mussolini.
Categoria de resultados
Mesmo com tamanha concorrência, o mercado de MIPs segue com números que causam inveja a outras classes medicamentosas e nem se compara a outros segmentos econômicos. Rendeu mais de R$ 19 bilhões de ganhos para indústria e varejo no ano de 2017, alcançando crescimento de 9,2% em um ano marcado por retrações e incertezas no País.
A categoria segue se expandindo porque há espaço para diversas versões de um mesmo medicamento. A combinação de aumento da renda dos brasileiros, ampliação do acesso à saúde privada e crescente envelhecimento da população fez do mercado farmacêutico brasileiro um terreno fértil. Entre 2011 e 2017, esse setor dobrou de faturamento segundo a IQVIA.
É diante desses números que as indústrias têm investido cada vez mais na categoria. Tanto na ampliação dos lançamentos como na melhora da execução no ponto de venda (PDV) e em ações de propaganda que visam aumentar a visibilidade dos medicamentos dentro das farmácias.
Há oito anos no Brasil, o laboratório Aspen Pharma confirma os bons resultados que a categoria de MIPs traz aos fabricantes, mesmo diante de forte disputa comercial. “Nosso desempenho está sendo muito bom neste ano fiscal. Estamos acima do resultado esperado em 11%, sendo que a participação dos produtos sem prescrição é de 8%”, releva o diretor de marketing da Aspen Pharma, Jackson Figueiredo.
Confirmado o potencial do mercado brasileiro, boa parte desses resultados é consequência de ótima performance em produtos que contam com concorrência de diversas outras marcas, como Leite de Magnésia de Philips (para trato de males gastrointestinais), Kwell (combate a lêndeas e piolhos) e Calman (trata sintomas de ansiedade, irritabilidade, entre outros).
A aposta em produtos já tradicionais faz, inclusive, parte dos planos comerciais da empresa. “A Aspen Pharma tem seguido estratégias eficazes com foco na aquisição de produtos tradicionais e maduros no mercado e no crescimento orgânico desses medicamentos. Alguns que fazem parte do portfólio da empresa se tornaram sucesso de vendas”, conta.
Como se dá o processo de inovação em Pesquisa & Desenvolvimento (P&D) de novas versões?
Embora seja mais fácil obter e utilizar os Medicamentos Isentos de Prescrição (MIPs), eles atendem a todos os padrões de qualidade, eficácia e segurança da Agência Nacional de Vigilância Sanitária (Anvisa), assim como os medicamentos controlados.
Uma vez que um laboratório decide investir em um molécula, ele precisa enfrentar três fases de pesquisa clínica antes de obter o registro do produto. Confira as etapas:
Pré-Clínica
Testes em laboratório (em situações artificiais e em animais) para verificar se a molécula pesquisada tem o potencial esperado.
CLíNICA
Fase I: primeira etapa de testes em seres humanos de uma medicação cuja eficácia foi comprovada em animais na fase pré-clínica. Nesta fase, a medicação é testada em pequenos grupos (de 20 a 100) de voluntários sadios.
Fase II (estudo Terapêutico-Piloto): o número de pacientes que participa nesta fase é maior (de 100 a 200) e os voluntários já possuem a doença a ser tratada.
Fase III: neste estágio, o novo medicamento é comparado com o tratamento-padrão existente. O número de pacientes mínimos é de aproximadamente 800; esses estudos, normalmente, são internacionais, em vários centros (multicêntricos).
Fase IV: os estudos são realizados para se confirmar que os resultados obtidos na fase anterior (Fase III) são aplicáveis em uma grande parte da população doente. Esta fase se dá após a aprovação do medicamento onde ele já é comercializado.
Fonte: Agência Nacional de Vigilância Sanitária (Anvisa)
Para 2018, a Aspen Pharma prevê um crescimento de 8% e uma das grandes apostas será o tradicional Leite de Magnésia de Phillips, agora em diferentes versões e sabores. A iniciativa de reinventar um clássico não é à toa.
“É um dos principais produtos da empresa e tem uma ótima performance no mercado, vendendo mais de 500 mil unidades por mês”, revela Figueiredo. “Estamos apostando em uma forte parceria com a nossa equipe de trade, apoiada em uma campanha focada, principalmente, em redes sociais, TV fechada e mobiliário urbano.”
Dentro da Merck, a estratégia de utilizar medicamentos ou ingredientes ativos que já são comprovados pela sua segurança e eficácia para lançar variações também é adotada. “Hoje, a lista de MIPs aprovados pela Anvisa é restrita há algumas classes e moléculas, desta forma, a inovação é mais restrita”, comenta a head of marketing da Merck Brasil, Roberta Farina.
Por isso, a empresa investe forte na promoção do Floratil – MIP líder no segmento de antidiarreicos – e também no Cebion, uma vitamina C bastante conhecida pela população no tratamento auxiliar para gripes e resfriados. Junto com um fitoterápico tópico para o tratamento de dor – uma aposta mais recente –, esse é o portfólio que tem recebido mais investimento e atenção dentro da Merck. “As categorias mencionadas continuam sendo cada vez mais procuradas pelos pacientes”, garante Roberta.
Para driblar a concorrência, a Pfizer Consumer Healthcare segue apostando nos medicamentos de maior saída da marca, mas, ao mesmo tempo, tenta explorar algumas oportunidades em alta.
“As principais apostas da empresa estão na personalização, ou seja, investimos para trazer produtos que atendam às necessidades específicas do consumidor, o que é uma tendência mundial”, explica o diretor de vendas e trade marketing da Pfizer, Silvio Silva.
Os últimos lançamentos da empresa foram na linha Centrum, que já existe há anos no mercado, mas agora com formulações que visam atingir públicos específicos, para cada perfil e momento da vida. Homens e mulheres com 50 anos de idade ou mais, além de pacientes preocupados em manter níveis saudáveis de triglicerídeos, são o atual foco dessa linha de multivitamínicos, uma vez que a população idosa brasileira tende a crescer vertiginosamente nas próximas décadas.
Foto: Shutterstock